近日,南方科技大学生命科学学院助理教授刘忠民课题组联合浙江大学生命科学学院百人计划研究员王勇课题组在国际著名学术期刊Nature Communications上发表了题为“Inhibition and transport mechanisms of the ABC transporter hMRP5”的研究论文。这项工作首次揭示了人源MRP5转运机制,并设计了靶向人源MRP5的多肽分子。相关的研究成果为MRP5特异性抑制剂的开发提供重要线索,对MRP5介导的肿瘤细胞多药耐药治疗研究具有重要的指导意义。
MRP(Multidrug resistance-associated protein)通过将抗癌药物外排到细胞外,从而降低细胞内药物浓度,在介导多药耐药过程中发挥关键作用,对有效治疗癌症造成了重要挑战。人源MRP5(human MRP5, hMRP5)作为MRP家族的一员,能够转运多种抗肿瘤药物,包括甲氨蝶呤、顺铂、嘌呤类似物、嘧啶类似物等。相关数据证实多种肿瘤细胞中呈现MRP5高表达的现象。MRP5在肿瘤多药耐药产生过程发挥重要作用,给癌症治疗带来挑战。因此,研究MRP5的转运工作机理具有重要的意义。同时,在癌症治疗的研究中,有证据表明MRP抑制剂联合抗癌药物可以提高疗效。然而,现有的小分子抑制剂存在亲和力弱、效率低、特异性和安全性差等问题。相关研究证实,多肽抑制剂有更广泛的结合界面、更高的安全性和更高的效率。然而,目前尚无靶向hMRP5的的多肽分子。因此,开发作用于MRP5的新型多肽抑制剂具有重要的医学意义。
研究团队利用单颗粒冷冻电镜技术解析人源MRP5在不同转运状态下冷冻电镜结构,研究发现在静息状态下,野生型MRP5呈现自抑制的构象,即由自身氨基端多肽结合其转运通道并抑制MRP5结合底物的构象,这是首个报道的由N端多肽自抑制的ABC转运蛋白三维结构。基于MRP5不同状态下的三维结构信息,研究团队进一步设计了靶向人源MRP5的多肽分子,并利用爪蟾卵母细胞转运体系证实所涉及的多肽分子M5PI可以有效抑制抗肿瘤药物分子阿霉素的外排。另外,研究团队还发现了人源MRP5的第一个核苷酸结合结构域中含有一个特殊的调节基序(R motif),进一步研究发现R motif通过与磷脂种类的结合偏好性在调控MRP5在细胞中的定位发挥重要功能。最后,基于结构、生化、细胞和分子动力学模拟等实验结果,研究团队提出了人源MRP5的转运工作模型(图1)。
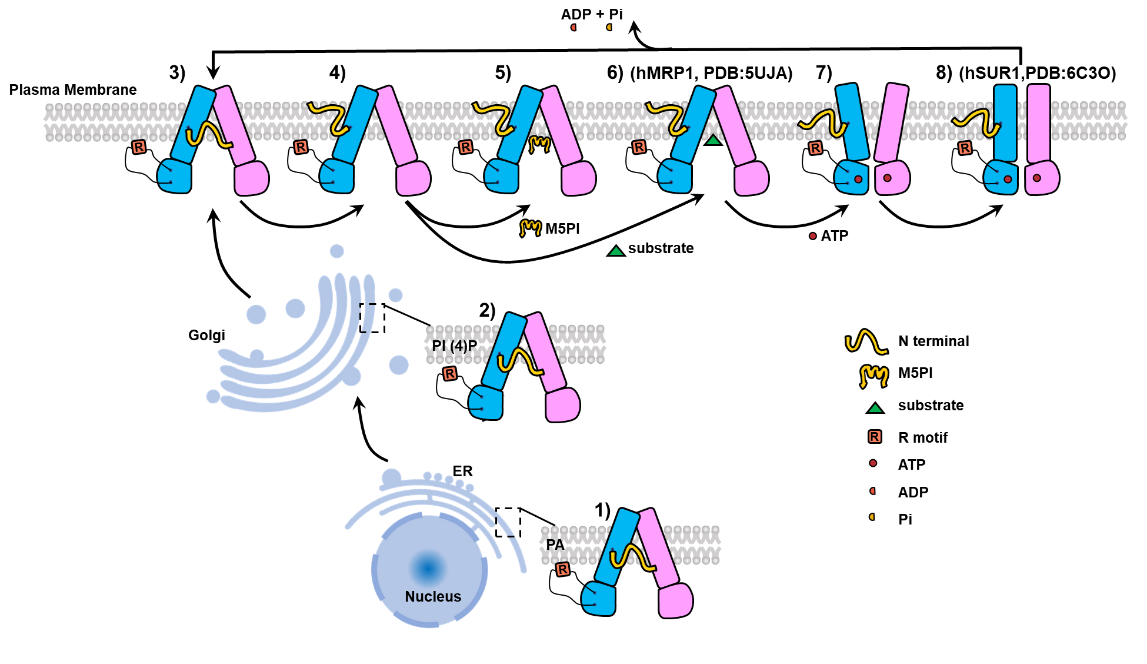
图1:人源MRP5的转运循环模型
总的来说,这项研究工作为理解人源MRP5转运抗肿瘤、抗病毒药物产生多药耐药性的分子机理提供了解释,为设计靶向MRP5的特异性抑制剂提供了基础。同时,这项工作首次报道了来自N端多肽自抑制的ABC结构,丰富了ABC转运蛋白家族的工作调控机制研究。因此,这项研究具有重要的生物医学意义。
南方科技大学刘忠民和浙江大学王勇为本论文共同通讯作者,南方科技大学为第一通讯单位。南方科技大学博士生黄颖、薛晨阳、卜瑞倩和吴藏为并列第一作者。南方科技大学生命科学学院副教授陈永龙、研究助理教授石照应、浙江大学李嘉辰、张晋秋和陈锦裕为该项研究的合作作者。冷冻电镜数据收集和处理得到了南科大冷冻电镜中心和水木未来的大力支持。该工作得到了国家自然科学基金、国家十四五重点研发计划“生物与信息融合”专项、深圳市科创委的资助。
论文链接:https://www.nature.com/articles/s41467-024-49204-1
转载自南科大新闻网


